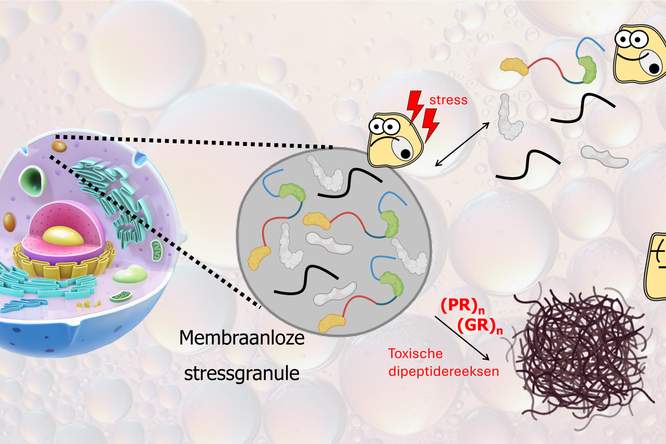
Een onderzoeksteam van VIB en KU Leuven heeft eiwitten ontdekt die bijdragen tot de ontwikkeling van ALS en fronto-temporale dementie (FTD). ALS en FTD zijn twee ongeneeslijke hersenziekten die worden gekenmerkt door neurodegeneratie, het abnormaal afsterven van hersencellen. In België lijden zo’n 1000 mensen aan ALS en 4000 aan FTD.
ALS en fronto-temporale dementie (FTD) zijn vrij zeldzaam en treffen slechts een beperkt aantal patiënten in België. Toch is de impact van deze ziekten bijzonder groot, zowel voor de patiënten als voor vrienden en familie. Bij ALS gaat de spierfunctie immers razendsnel achteruit, waardoor patiënten gradueel de controle over hun lichaam verliezen. Patiënten met FTD verliezen dan weer hun cognitieve functies en vertonen gedragsveranderingen waarbij ook het geheugen achteruitgaat.
Sommige mensen vertonen een overlap van symptomen van zowel ALS als FTD. Dit komt doordat beide aandoeningen kunnen veroorzaakt worden door een mutatie in het C9orf72-gen. Hoe deze mutatie precies tot de ziektes leidt, bleef tot nu toe echter nog onduidelijk. Nu heeft een Leuvens onderzoeksteam onder leiding van professor Ludo Van Den Bosch (VIB-KU Leuven Centrum voor Hersen- en Ziekteonderzoek) drie eiwitten, NEK6, HNRNPK en RRM2, ontdekt die een rol spelen in het ziekteproces van deze familiale variant van ALS en FTD. De ontdekking van deze eiwitten baant de weg voor nieuwe therapeutische strategieën voor het behandelen van deze aandoeningen.

Ludo Van Den Bosch (VIB-KULeuven): "Deze bevindingen vormen zowel een wetenschappelijke als technische doorbraak op het gebied van het dementieonderzoek. Ons onderzoek draagt zeker bij tot de ontrafeling van de ziektemechanismen van ALS en FTD, en, hopelijk, tot het vinden van een remedie voor deze dramatische aandoeningen."
Doorbraken dankzij unieke technologieën
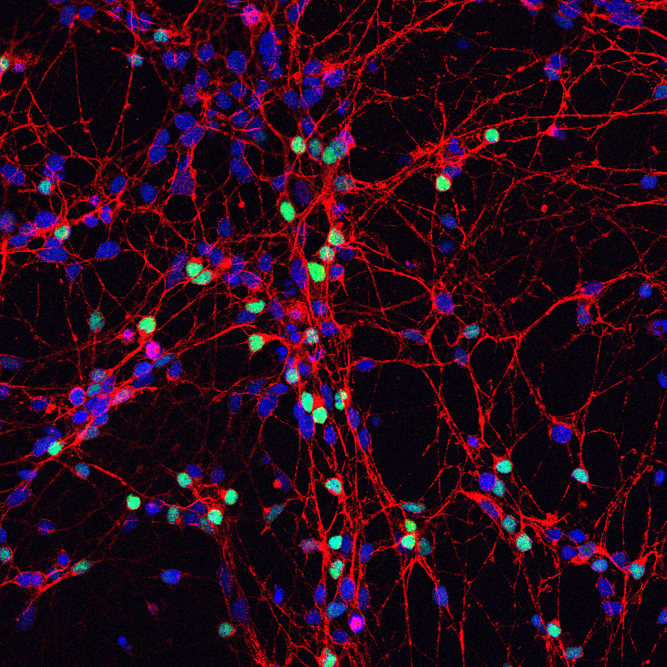
Postdoctoraal onderzoekster Wenting Guo en haar team in het labo van Ludo Van Den Bosch ontdekten dat het onderdrukken van het eiwit NEK6 de DNA-schade in neuronen terugdraaide en de toxische effecten van de C9-mutatie tegenging. De ontdekkingen werden gedaan door middel van een screening met CRISPR-Cas9 en humane stamcellen, een wereldprimeur. Deze studie werd uitgevoerd in samenwerking met het Stamcelinstituut Leuven (SCIL).

Professor Catherine Verfaillie, hoofd van het SCIL, licht toe: "Door gebruik te maken van stamcellen is er voor het eerst een menselijk model beschikbaar om de mechanismen te bestuderen die aan de basis liggen van neuronale celdood en om kandidaat-geneesmiddelen te testen voor ziektes zoals ALS en FTD."
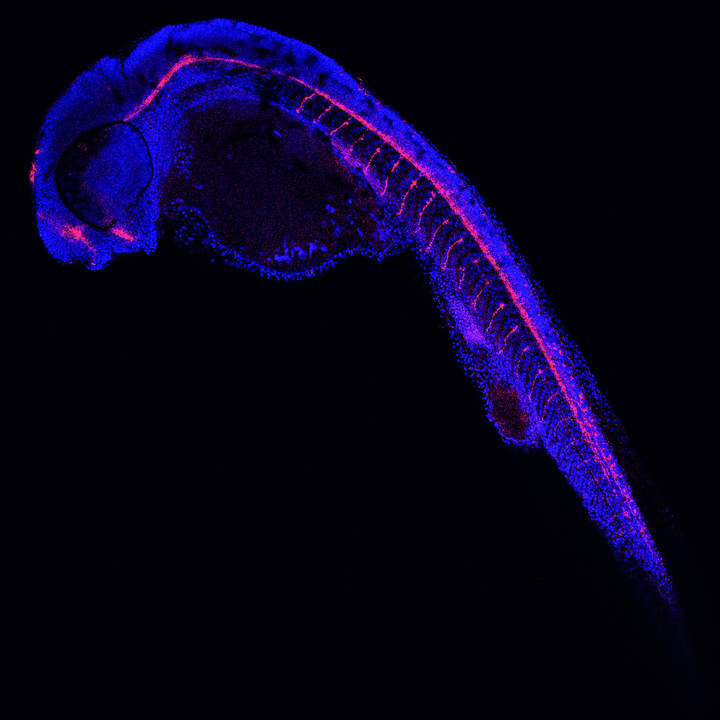
Doctoraatsstudent Elke Braems en haar collega’s ontdekten dan weer dat de HNRNPK-en RRM2-eiwitten essentieel zijn voor het handhaven van een effectieve DNA-schaderespons bij een C9-mutatie. Deze eiwitten activeren in patiënten met genetische ALS en FTD kan dus een nieuwe therapeutisch strategie vormen. De resultaten werden aangetoond in een zebravismodel en geverifieerd in menselijke stamcellen en stalen van patiënten in samenwerking met het UZ Leuven.
Ludo Van Den Bosch: "De NEK6, HNRNPK, en RRM2 eiwitten vormen veelbelovende doelwitten voor medicijnen voor ALS en FTD, maar eerst moeten we hun mechanismen verder begrijpen. Daarna is meer onderzoek nodig naar de ontwikkeling van betrouwbare NEK6-remmers en HNRNPK- en RRM2-activatoren."

Meer weten?
Als je meer wil weten over hersenonderzoek of hersenaandoeningen, bekijk dan zeker onze educatieve pagina’s, zoals ons dossier Alzheimer en hou onze website in de gaten voor het laatste nieuws of meer informatie over lezingen waar je uit eerste hand meer kan horen over wat onze onderzoekers bezighoudt.
Wie graag mee wil werken aan onze missie om de mysteries van onze hersenen te ontrafelen kan een kijkje nemen bij onze vacatures.
Ontdek meer van VIB Neuroscience in de kijker op de webpagina.