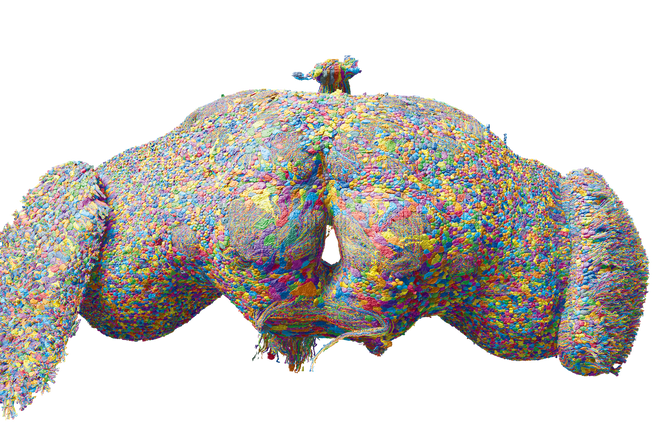Het menselijke genoom bestaat uit ongeveer twintigduizend genen. Elk gen bevat de code die bepaalt hoe je eruitziet en hoe je lichaam werkt, maar helaas ook de ‘foutjes’ die leiden tot het ontstaan van een erfelijke aandoening. De geniale handleiding is geschreven in een taal die we lang niet begrepen, en vandaag nog altijd aan het ontcijferen zijn.
Halverwege de negentiende eeuw ontrafelde een jonge monnik in een klooster in Brno, in wat nu Tsjechië is, de eerste stukken van de inhoudstafel. Gregor Mendel (1822-1884) hield van de natuur en van wiskunde, en telde daarom zowat alles wat hij zag. Aanvankelijk kweekte hij muizen, keek naar hun fysieke eigenschappen, en telde hoe vaak en op welke manier die eigenschappen bij het nageslacht terug verschenen.

Omdat de bisschop zijn bedenkingen had bij een monnik die hele dagen naar seksende muizen zat te kijken, verlegde Mendel zijn focus naar de erwtenplanten in de kloostertuin. Zeven jaar lang kruiste hij erwtenplanten die slechts in één eigenschap van elkaar verschilden, zoals een plant met groene zaden en een met gele zaden. Hij poederde het stuifmeel van de mannelijke bloem van de ene plant naar de vrouwelijke bloem van de andere. Het nageslacht, dat Mendel de F1-generatie noemde, produceerde enkel gele erwten.
Toch waren de groene erwten niet verdwenen, want de generatie daarop, F2, doken ze terug op in een verhouding van drie gele tegenover één groene erwt. Mendel zag die logica ook bij andere eigenschappen, zoals bloemkleur en textuur van de erwten. Hij leidde uit zijn waarnemingen af dat de eigenschappen van zijn erwten werden bepaald door twee ‘factoren’ afkomstig van beide ouders, dat de ene factor ondergeschikt kon zijn aan de andere, maar in de daaropvolgende generatie toch weer kon opduiken. Die factoren noemen we nu genen.
Gregor Mendel promoveerde na het tellen van zijn driehonderdduizendste erwt tot abt van het klooster (het een had niets met het andere te maken), en zijn inzichten bleven een halve eeuw onzichtbaar voor de wetenschap. Pas in het begin van de twintigste eeuw herontdekten onderzoekers Mendels basisregels van de genetica.
Dat de generaties bij de fruitvlieg elkaar zo snel opvolgen, is uiteraard handig als je erfelijke aandoeningen bestudeert
Onder hen de Amerikaanse geneticus Thomas Morgan (1866-1945). Hij wou achterhalen of de eenvoudige erfelijkheidswetten ook op dieren van toepassing zijn. Hij zocht daarvoor een geschikt modelorganisme dat hij makkelijk in het lab kon huisvesten en dat zich snel en in grote aantallen kon reproduceren. En toen landde een fruitvlieg op de banaan die zijn vermoeide hersenen van brandstof moest voorzien. Pats! Tot zover de romantisering. Of het echt een verpletterde fruitvlieg was die het startschot inluidde, weten we niet, maar het is wel een feit dat Morgan met zijn keuze voor de fruitvlieg het revolutionaire tijdperk voor de genetica, waarin we ons vandaag nog bevinden, opende. In een klein kamertje op de Amerikaanse Columbia University verzamelde Morgan bananen en lege melkflessen, en startte met het kweken van fruitvliegen. Het kamertje stond snel bekend als de Fly Room.
Oogcontact van de geniaalste soort
Net zoals Mendel kruiste Morgan generatie na generatie op zoek naar erfelijke patronen. Bij fruitvliegen ging dat net iets makkelijker dan bij erwten. De insecten kweken als konijnen, maar dan vaker en sneller. Een fruitvliegvrouwtje legt gemiddeld tweehonderd eitjes, en na amper tien dagen is haar kroost klaar om hetzelfde te doen. Dat de generaties elkaar zo snel opvolgen, is uiteraard ontzettend handig als je erfelijke aandoeningen bestudeert.
Op een dag in 1910 keek Morgan door een lens naar een mannelijke fruitvlieg, en het viel hem op dat het beestje witte in plaats van de normaal rode ogen had. Wanneer hij dat mannetje liet paren met vrouwtjes met rode ogen, dan hadden alle nakomelingen terug rode ogen. Nog een generatie later hadden de fruitvliegen zowel witte als rode ogen, in een verhouding van drie vliegen met rode tegenover één vlieg met witte ogen – net zoals bij de erwten van Mendel dus. De vliegen met witte ogen waren wel allemaal mannetjes, net zoals hun grootvader. Morgan bevestigde dus niet alleen de inzichten van Mendel, hij merkte ook dat mannen op een ietwat andere manier eigenschappen overerven dan vrouwen. Hij verklaarde dit door te stellen dat genen op chromosomen liggen, en dat mannetjes maar één versie van zo’n chromosoom (het X-chromosoom) hebben, terwijl vrouwelijke fruitvliegjes er twee hebben. Dit betekent dat mannelijke fruitvliegjes maar één kopie van het gen voor rode oogkleur hebben, terwijl vrouwelijke fruitvliegjes er twee hebben. Vrouwtjes met een ‘kapot’ gen voor rode oogkleur hadden, in tegenstelling tot mannetjes, nog altijd een reservegen. Daarom hadden vrouwtjes nooit witte ogen, tenzij ze op elk chromosoom een ‘kapot’ gen droegen.
Fruitvliegconsortium
Morgan was een van de eerste wetenschappers die de woorden genen en chromosomen gebruikte, en de structuur ervan in kaart bracht. Zijn onderzoek werd in 1933 terecht bekroond met de Nobelprijs, en maakte genetische modificatie en gentherapie mogelijk. De fruitvlieg, Drosophila melanogaster, werd zo een blijver in het lab.
Intussen, na meer dan honderd jaar onderzoek, hielp de simpele fruitvlieg wetenschappers grote stappen zetten in onder andere genetica, embryologie, celbiologie en neurowetenschappen, en redde zo miljoenen mensenlevens. ‘Er zijn weinig organismen waar we zoveel vanaf weten als van de fruitvlieg’, zegt bio-ingenieur Stein Aerts van de KU Leuven en het VIB. Hij ontwikkelde samen met fruitvliegexperts van over de hele wereld de Fly Cell Atlas, een gedetailleerde kaart van alle celtypes van de volwassen fruitvlieg, inclusief hersencellen, spiercellen, immuuncellen en de gespecialiseerde cellen betrokken bij zien, horen, ruiken, proeven en voelen.
Het idee voor de Fly Cell Atlas ontstond in 2017 op een internationaal fruitvliegcongres – ja, dat bestaat echt – en groeide intussen uit tot een groot internationaal fruitvliegconsortium. ‘We ontwikkelen eigenlijk een lijst van alle genen die actief zijn in specifieke cellen. Onderzoekers die een specifiek orgaan, weefsel of cel willen onderzoeken, kunnen in de Fly Cell Atlas opzoeken welke genen betrokken zijn. Er is ook een Human Cell Atlas in de maak dat ongeveer hetzelfde doel heeft, maar dat zal veel langer duren.’
Mensen zitten veel complexer in elkaar, en wetenschappers kunnen ook niet zomaar onderzoeken wat ze willen bij mensen – en maar goed ook. ‘We kunnen geen mutaties aanbrengen in de genen van een mens, of we kunnen niet tijdens iemands leven dissecties uitvoeren om evoluties in weefsels op te volgen. Voor fundamentele principes die zich afspelen in levende organismen gebruiken we daarom modelorganismen. Bijvoorbeeld de basiswetten van genetica gelden in alle levende organismen. Hoe werkt DNA? Welke informatie zit erin geprogrammeerd, en hoe? En op welke manier vertaalt DNA zich in een functie? Dat soort vragen kunnen we ook met behulp van een modelorganisme beantwoorden.’
Een dollar voor een fruitvliegmutant
Uiteraard kies je als wetenschapper dan best een modelorganisme dat praktisch is. ‘Drosophila melanogaster is niet groter dan een rijstkorrel. Je kunt ze huisvesten in kleine glazen of plastic tubes met wat voedsel in. Ze planten zich ook razendsnel voort. Dit betekent dat we snel en gemakkelijk kunnen observeren hoe veranderingen in het genetisch materiaal een effect hebben op de ontwikkeling, het gedrag en het ontstaan van aandoeningen. Dat ze hoogstens zestig dagen leven is dan weer interessant om veroudering en ouderdomsziektes te bestuderen. Ook fruitvliegen vertragen bijvoorbeeld op een manier die vergelijkbaar is met wat er bij mensen gebeurt.’
‘Er zijn geen wettelijke bepalingen rond fruitvliegen, wat bij ‘hogere’ modelorganismen wel het geval is. En je kan met een klein budget een laboratorium opstarten om state of the art onderzoek te doen. Een microscoop en wat fruitvliegen volstaan. We halen de vliegen in stockcenters met collecties van genetisch gemodificeerde fruitvliegen, waar je voor een dollar al een buisje vol vliegen met het gendefect dat je wil bestuderen kunt kopen. Er bestaan tienduizenden genetische varianten van de fruitvlieg. Het genoom van de fruitvlieg telt vijftienduizend genen, en er bestaan fruitvliegvarianten met telkens een van die genen uitgeschakeld. Door elk gen apart uit te schakelen, weten we welke informatie het gen bevat. Eenvoudig gezegd, als een bepaalde eigenschap niet meer tot uiting komt met gen dertienduizend uitgeschakeld, dan weten we dat gen dertienduizend betrokken is bij het ontstaan van die eigenschap.’
Heel wat fruitvliegonderzoekers delen hun collecties ook bijna gratis met elkaar. ‘Als een wetenschapper de genen van een fruitvlieg met behulp van crispr heeft aangepast, dan kan die mutant ook naar een stockcentrum worden gestuurd, en van daaruit weer naar andere onderzoekers. Zo gaan er continu pakketjes met fruitvliegen de wereld rond. Als ze wat langer onderweg zijn, versturen we enkel eitjes. Die kunnen zich tijdens de reis al ontwikkelen en bij aankomst zijn het misschien al larven of poppen.’
Levende petrischalen
Heel wat praktische voordelen dus, maar ook als onderzoeksobject heeft de fruitvlieg bijna ideale eigenschappen – hoewel het insect dus eigenlijk toevallig in de wetenschap terecht is gekomen. ‘Om complexe zaken te begrijpen, begin je best bij het eenvoudige. Dat principe geldt zeker voor de fruitvlieg. Drosophila heeft een heel mooi genoom. Het is compact, twintig keer kleiner dan het menselijke genoom. Onze genen hebben drie of vier kopieën. Als je die wil bestuderen, moet je ze een voor een verwijderen om de functie ervan na te gaan. De fruitvlieg heeft maar één kopie van elk gen, dat vergemakkelijkt het onderzoek. Drosophila heeft ook maar vier chromosomen. Alles is compacter en eenvoudiger.’

Dankzij die genetische eenvoud kunnen wetenschappers sneller zien welke genen verantwoordelijk zijn voor welke eigenschappen. Stein Aerts: ‘Ik kan makkelijk tienduizenden vliegen met hetzelfde genotype kweken, snel de effecten van een mutatie beoordelen en leren wat er fout gaat op cellulair niveau. Dat is vooral nuttig als we de genetische onderbouwing van menselijke ziekten onderzoeken. Dankzij genoomstudies bij mensen krijgen we verdachte genen in het vizier. Sommige daarvan zullen echt betrokken zijn bij het ontstaan van een ziekte, andere niet. Fruitvliegen bieden een platform om die verdachten te beoordelen en de echte boosdoeners te identificeren. Nadat we hebben vastgesteld wat een gen doet in een fruitvlieg, kunnen we op zoek gaan naar soortgelijke genen in complexere organismen en rationele hypothesen maken over hun activiteit.’
Neen, fruitvliegen zijn niet gewoon simpele mensjes met vleugels. Toch hebben we veel meer met elkaar gemeen dan je zou denken. ‘Omdat het leven op aarde een gemeenschappelijke voorouder heeft, delen we veel van onze genetica en bijna al onze biochemie. Een fruitvlieg heeft net zoals een mens nieren, een darm en een hart. Anderzijds missen ze bloedvaten en maken ze geen antilichamen aan om ziektes te bestrijden. Je kan dus niet alle biologische systemen bestuderen in Drosophila, maar de fundamentele concepten van DNA, cellen, eiwitten, celcommunicatie, organen wél. Zo’n zestig procent van de genen die geassocieerd zijn met menselijke aandoeningen komen ook voor bij fruitvliegen. Als je bijvoorbeeld de risicogenen voor de ziekte van Parkinson uitschakelt, zie je ook bij fruitvliegen motorische problemen.’
Zo maak je een fruitvliegmutant
Om de functie van een specifiek gen te achterhalen, kunnen onderzoekers enkel dat gen in het genoom van een fruitvlieg uitschakelen en zien wat de gevolgen zijn. Ze doen dat niet in de volwassen fruitvliegen, maar in de embryo’s. Stel dat je veroudering bestudeert en wil achterhalen welke genen betrokken zijn, dan kan je elk gen een voor een uitschakelen en zien of de fruitvliegen die zich uit de gemodificeerde embryo’s ontwikkelen langer of korter leven dan gemiddeld. Wetenschappers maakten daarom al tienduizenden labvarianten van de wilde fruitvlieg, telkens met iets andere genen. Hoe ze dat doen is een ingewikkeld proces, maar toch een poging: het begint meestal met DNA.
Wetenschappers stoppen het DNA dat ze willen onderzoeken eerst in een plasmide, een klein circulair stukje DNA dat je (erg vereenvoudigd) kan zien als een enveloppe (de plasmide) met een brief (het DNA) in. De ontvanger van de brief (in dit geval het DNA van de fruitvlieg) kan de brief openen, de informatie lezen en doen wat erin wordt gevraagd. Wetenschappers keken deze methode af van de bacteriën, die plasmiden gebruiken om losse genetische elementen met elkaar te delen. Tot hier komt er nog geen fruitvlieg aan te pas, wel een pipet en kleine mengbuisjes. De wetenschappers sturen de plasmide vervolgens op naar een gespecialiseerd laboratorium, waar ze de ‘enveloppe’ injecteren in een embryo van een fruitvlieg. Om te controleren of de gentransfer is gelukt, wordt een merkergen aan het stukje DNA gekleefd. Dat merkergen is meestal gelinkt aan de oogkleur van de vlieg. Als het nageslacht rode ogen heeft, weten de onderzoekers dat het nieuwe DNA succesvol is ingevoerd – een ‘trucje’ dat doet denken aan die ene vlieg met witte ogen die pionier Thomas Morgan onder zijn microscoop zag verschijnen. De genetisch gemodificeerde vliegen keren dan terug naar het oorspronkelijke lab, waar ze verder worden gekweekt en bestudeerd.
Hersenen peuteren
De hersenen van de fruitvlieg zien er anders uit dan de onze, maar opnieuw zijn de fundamentele principes gelijkaardig. Stein Aerts: ‘Ook fruitvlieghersenen bevatten zenuwcellen die connecties met elkaar maken, en hersendelen activeren of onderdrukken. Als je wil achterhalen hoe een neuron werkt, kan je dat ook in de hersenen van een fruitvlieg doen. De insecten hebben ook receptoren, bijvoorbeeld voor geur en tast, die informatie sturen naar de hersenen.
In de hersenen worden die signalen verwerkt en aan andere zaken gelinkt, zoals geheugen of leren. Vanuit de hersenen ontstaat dan ook vraag naar een bepaalde actie in bijvoorbeeld de spieren. Het totale proces van input, verwerking en output is dus gelijkaardig in mensen- en fruitvliegbreinen. Maar hersenen van de fruitvlieg bestaan uit ‘slechts’ 250.000 zenuwcellen, terwijl de menselijke hersenen uit vele miljarden cellen zijn opgebouwd. Het brein van de fruitvlieg is dus beduidend eenvoudiger en overzichtelijker.
Omdat de hersenen van de fruitvlieg zo klein zijn, kunnen wetenschappers ze in hun totaliteit bekijken onder de microscoop. ‘Als je de connecties tussen hersencellen moet bestuderen bij mensen of muizen, dan is je gezichtsveld onder de microscoop altijd beperkt omdat je slechts fragmenten van de hersenen kunt bekijken. Het brein van de fruitvlieg is zo klein dat het in één stuk onder de microscoop past. Meer zelfs, we kunnen soms tot twintig hersenen tegelijk onder een microscoop bekijken.’
Kleiner betekent wel verfijnder handwerk. ‘Om de hersenen onder de microscoop te kunnen bekijken, moeten we ze eerst uit de kop van de fruitvlieg halen. Dat is een erg precies werkje, en je moet binnen de minuut klaar zijn. Daarna zijn de hersenen niet meer bruikbaar voor onderzoek. Als fruitvliegonderzoeker moet je dus wel behoorlijk wat oefenen vooraleer je echt aan de slag kunt.’
Een fruitvlieg met geheugen
Als je intussen nog niet onder de indruk bent van de capaciteiten van de fruitvlieg, dan proberen we het nu nog eens: die simpele fruitvlieg heeft een geheugen, een vrij goed geheugen zelfs. Wetenschappers kunnen het geheugen zelfs trainen met behulp van geuren. Een fruitvlieg die eerst iets ruikt en dan een elektrische schok krijgt, zal die geur daarna ontwijken, zelfs enkele dagen later nog. Krijgt de fruitvlieg bij een andere geur een suikerrijke beloning, dan zal hij of zij die geur daarna terug opzoeken, ook zonder beloning. Als hersenonderzoeker kan je in de hersenen van zo’n getrainde fruitvlieg kijken hoe die geur in de hersenen wordt vertaald naar een herinnering.
De eerste keer dat een gen gelinkt aan geheugen werd ontdekt, was trouwens bij de fruitvlieg. En in 2004 ontvingen Richard Axel en Linda Buck de Nobelprijs voor Geneeskunde, voor hun ontdekking van het reukvermogen en de moleculaire basis ervan. Ze ontdekten hoe specifieke geuren worden herkend door de geurreceptoren in de voelsprieten en hoe deze informatie wordt doorgegeven aan de hersenen. Ze kregen hun inzichten dankzij onderzoek bij fruitvliegen. Ook de werking van de biologische klok, waarmee organismen zich aanpassen aan het dag- en nachtritme op aarde, werd grotendeels ontrafeld dankzij onderzoek bij fruitvliegen (nog een Nobelprijs, dit keer voor Jeffrey Hall, Michael Rosbash en Michael Young in 2017).
We delen veel van onze genetica en bijna al onze biochemie. Een fruitvlieg heeft ook nieren, een darm en een hart
Dat je het geheugen van fruitvliegen kunt trainen, is bijzonder interessant voor onderzoek naar hersenaandoeningen. ‘Wetenschappers kunnen bijvoorbeeld bestuderen hoe dementie zich ontwikkelt, door mutaties te creëren die leiden tot abnormale ophoping van eiwitten in de hersenen van de fruitvliegen. Vervolgens kunnen ze de effecten van deze mutaties onderzoeken, bijvoorbeeld door te kijken naar veranderingen in het vermogen van de fruitvliegen om te leren en te onthouden. Fruitvliegen worden ook gebruikt om potentiële behandelingen voor dementie te testen. Wetenschappers kunnen bijvoorbeeld bepaalde medicijnen of andere stoffen toedienen aan fruitvliegen met de mutaties die leiden tot dementie-achtige symptomen, om te zien of deze stoffen de symptomen verminderen.’
De fruitvlieghersenen kunnen ons dus nog ontzettend veel leren over de werking van ons brein en lichaam, maar daarvoor moeten we eerst ook nog ontzettend veel leren over de hersenen van de fruitvlieg. De Fly Cell Atlas is daarom nu al aan een upgrade toe. Stein Aerts: ‘We hebben alle celtypes van de fruitvlieg in kaart gebracht, maar we kunnen ze nog niet allemaal lokaliseren in het lichaam van de fruitvlieg. Eigenlijk hebben we het beest uiteengetrokken in duizenden puzzelstukjes en dan van elk puzzelstukje een analyse gemaakt. De puzzel opnieuw in elkaar steken kunnen we nog niet, omdat we niet weten waar elk stukje zich bevindt. We willen daarom nu alle celtypes visualiseren in een complete fruitvlieg, en de cellen dus identificeren waar ze zich bevinden in het lichaam. Dan gaan we van een atlas naar een stafkaart van de fruitvlieg.’
‘Zo’n kaart zal ons helpen om op langere termijn aandoeningen bij mensen op celniveau te bestuderen, en dus niet langer op het weefselniveau alleen. In een orgaan of weefsel zitten een bundel van verschillende celtypes, maar niet al die celtypes zijn betrokken bij een aandoening. Als we op celniveau kunnen kijken, kunnen we dus ook die aandoeningen veel preciezer gaan behandelen. We zullen dan kunnen zien wat individuele kankercellen of immuuncellen van een patiënt doen, en dan strategieën ontwikkelen om op dat niveau een veel nauwkeurigere impact te hebben. En dat allemaal dankzij de fruitvlieg.’