Wat als je in het ziekenhuis belandt met een zware griepinfectie? Wat als je daarbovenop een schimmelinfectie ontwikkelt? Een dubbele uitdaging met slechts vijftig overlevingskans. Immunotherapie kan dan een oplossing bieden.
Schimmels zoals Aspergillus zijn overal te vinden in onze omgeving, van de prachtige paddenstoelen in onze bossen, de paddenstoelendelicatessen op ons bord tot schimmels die groeien in onze koelkasten. Ze zijn zo talrijk aanwezig in onze wereld dat we elke dag honderden tot duizenden schimmelsporen inademen. Deze schimmelsporen worden makkelijk verwijderd uit de longen door het immuunsysteem bij gezonde mensen, maar ze kunnen ons lichaam teisteren en volledig besmetten als het immuunsysteem verzwakt is. Door de opwarming van de aarde zou het kunnen dat sommige schimmels zich aanpassen aan hogere temperaturen, waardoor ze beter kunnen overleven bij de lichaamstemperatuur van mensen. Hierdoor kunnen ze gevaarlijk worden en ziektes bij mensen veroorzaken. Om de strijd tegen de schimmels aan te scherpen, heeft de Wereldgezondheidsorganisatie, de WHO, recent een lijst met de meest zorgwekkende schimmels gepubliceerd waaronder Aspergillus fumigatus. Recent werd duidelijk dat ook gezonde mensen in welbepaalde omstandigheden het doelwit kunnen worden van een dodelijke schimmelinfectie.
Hoesten, hoofdpijn, spierpijn, koorts… Elk jaar worden mensen over de hele wereld getroffen door griep. De griep, veroorzaakt door het influenzavirus, treft elk jaar gemiddeld 500 000 mensen in België1 en is dus zeker geen onschuldige infectie. Bij gemiddeld 1 op 1000 mensen die griep krijgen, doen zich complicaties voor, zoals ernstige longinfecties met ademhalingsproblemen1. Dit kan leiden tot een ziekenhuisopname, en in sommige gevallen zijn zelfs intensieve zorgen noodzakelijk. Welnu, ernstige griep werd onlangs geïdentificeerd als een risicofactor voor het ontwikkelen van een potentieel dodelijke, bijkomende schimmelinfectie. Een op vijf patiënten met ernstige griep op intensieve zorgen ontwikkelt een schimmelinfectie met Aspergillus in de longen. Dit heet ‘influenza-geassocieerde pulmonale aspergillose’ of korter: IAPA. Ondanks de geneesmiddelen die gebruikt worden tegen het griepvirus en de schimmel hebben die patiënten slechts vijftig procent kans om te overleven. Ook bij covid-19 hebben we gezien dat duizenden ernstig zieke Belgen een gevaarlijke schimmelinfectie ontwikkelden. Niet alleen in België, maar over heel de wereld wordt de connectie gelegd tussen een ernstige virale longinfectie (griep & covid-19) en invasieve schimmels, vaak met fatale gevolgen. Het gebrek aan effectieve behandelingsstrategieën maakt de situatie des te nijpender.
In onze zoektocht naar aanvullende behandelingen voor patiënten met IAPA, zijn analyses op patiëntstalen en proefdieren heel belangrijk om nieuwe inzichten te krijgen. Daarom heeft ons team IAPA bij muizen bestudeerd.
We zien dat die combinatie van griep en een schimmelinfectie bij muizen vergelijkbaar verloopt als bij mensen. Er kunnen ook ernstige ontstekingen, schade en schimmelinfecties in hun longen optreden. Daarnaast hebben we laten zien dat de huidige antivirale medicijnen, zoals oseltamivir en baloxavir marboxil, de ernst van de griep kunnen verminderen, wat ook de kans op de dodelijke schimmelinfectie kleiner maakt2,3. Idealiter worden die antivirale geneesmiddelen in een zeer vroeg stadium van de griepinfectie toegediend om een dodelijke schimmelinfectie te vermijden. De behandeling vroeg starten is dus de boodschap. De realiteit is echter dat deze vroege fase vaak al lang gepasseerd is bij grieppatiënten die in het ziekenhuis worden opgenomen. Ook geneesmiddelen tegen schimmels zijn soms niet efficiënt genoeg om de schimmel onder controle te krijgen. Daarnaast doet zich het toenemende probleem voor van schimmels die resistent zijn tegen de huidige schimmelwerende middelen. Dus antivirale en schimmelwerende geneesmiddelen zijn goed, maar niet goed genoeg.

Om patiënten met een griep- en schimmelinfectie een betere overlevingskans te bieden, is het van cruciaal belang dat we op zoek gaan naar meer doeltreffende geneesmiddelen. Hiervoor moeten we begrijpen hoe griep ons afweersysteem manipuleert, zodat het afweersysteem tijdelijk niet in staat is om ons adequaat te beschermen tegen de invasie van schimmels. Onze afweerrespons tegen infecties is een ingewikkeld immunologisch proces dat via verschillende stappen tot stand komt. Tot op de dag van vandaag blijft het ontcijferen van deze immunologische code een uitdaging. Nochtans kan kennis over de immunologische code ons helpen te bepalen of we immunomodulerende geneesmiddelen (ook wel immunotherapie genoemd) in ons arsenaal hebben die ons immuunsysteem kunnen ondersteunen bij het bestrijden van de schimmel, bovenop de antischimmelmedicatie.
Door verschillende immunologische technieken te gebruiken bij de muizen met zowel een griep- als schimmelinfectie, zijn we erin geslaagd om een deel van de immunologische code te ontcijferen. Nu begrijpen we beter hoe griep ons afweersysteem manipuleert, waardoor het ons niet meer afdoende kan beschermen tegen de dodelijke schimmel4. Inderdaad, ten eerste beschadigt griep de epitheelbarrière. De epitheellaag in onze longen vormt de eerste verdedigingslinie tegen schadelijke indringers zoals virussen, bacteriën en schimmels die we dagelijks inademen. Griep beschadigt deze fysieke barrière en opent op die manier de poorten voor de schimmel om in de longen binnen te dringen.
Eens binnengedrongen zorgt ons immuunsysteem ervoor dat de indringers opgeruimd worden. Als reactie op de griep en de schimmel produceert ons immuunsysteem alarmsignalen: eiwitten genaamd cytokines. Die cytokines zijn eigenlijk de boodschappers die ervoor zorgen dat een juiste immuunrespons tegen de griep en schimmel gestart wordt. Bij griep hebben we echter gezien dat ons immuunsysteem te sterk reageert en te veel cytokines produceert waardoor de immuunrespons tegen de schimmel niet goed meer werkt. Een van die cytokines die in grote hoeveelheden worden aangemaakt tijdens de griep is interferon gamma (IFN-γ). IFN-γ helpt normaal gesproken het lichaam om infecties te bestrijden door immuuncellen, zoals macrofagen en T-cellen, te activeren. Maar als er te veel IFN-γ wordt geproduceerd, raakt dit proces verstoord en werken deze macrofagen en T-cellen niet goed meer, waardoor ze niet meer in staat zijn om ons te beschermen tegen schimmelinfecties4. 'Overdaad schaadt’, zelfs bij afweer. Hierdoor kan griep ervoor zorgen dat we onszelf niet meer kunnen beschermen tegen een schimmelinfectie, waardoor de kans op een ernstige longziekte toeneemt.

Om het immuunsysteem te bestuderen, gebruiken we flowcytometrie, een techniek die ons in staat stelt om individuele cellen te identificeren. Rechts zie je het resultaat van deze analyse in longen van gezonde muizen en muizen met IAPA. In het beeld is een zwart kader weergegeven dat de immuuncellen aangeeft die positief zijn voor IFN-γ. Wanneer we de immuuncellen van gezonde muizen (blauwe stippen in het kader aan de linkerkant) vergelijken met de immuuncellen van de zieke IAPA-muizen (blauwe stippen in het kader aan de rechterkant), valt op dat de immuuncellen van gezonde muizen weinig IFN-γ produceren. Dit zien we terug in het aantal blauwe stippen in het kader: links zijn er weinig blauwe stippen, terwijl er rechts veel meer blauwe stippen te zien zijn. Dit duidt op een aanzienlijke toename van IFN-γ in de zieke IAPA muizen.
Nu we beter begrijpen hoe griep ons immuunsysteem beïnvloedt en daarmee een deel van de immunologische code hebben gekraakt, rijst de vraag of we IFN-γ-cytokine ook kunnen gebruiken als therapeutisch aangrijpingspunt voor het behandelen van IAPA met immuuntherapie. Immuuntherapie is een behandeling waarbij medicijnen worden gebruikt om ons immuunsysteem weer in balans te brengen. Dit kan door de overmatige productie van bepaalde cytokines, zoals IFN-γ, te remmen of hun werking te blokkeren. In onze studie hebben we genetisch gemodificeerde dieren gebruikt die geen of minder IFN-γ aanmaken. We konden zien dat door het verlagen van de IFN-γ productie de defecten in het immuunsysteem verdwenen waardoor de dieren zich konden verweren tegen de schimmelinfectie. De dieren waren beter beschermd tegen IAPA en waren beduidend minder ziek, wat suggereert dat het verlagen van IFN-γ de balans in het immuunsysteem kan herstellen4.
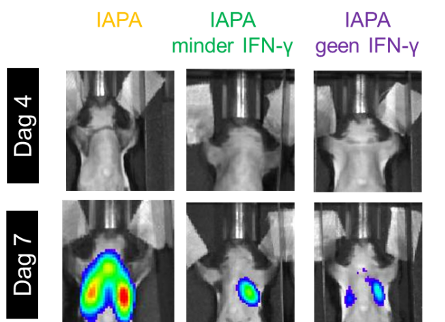
Om de schimmelinfectie te volgen in de longen van geïnfecteerde muizen, gebruiken we een genetisch gemodificeerde schimmel die licht produceert, een proces dat bioluminescentie wordt genoemd. Dit licht meten we met een speciale camera. Vier dagen na griepinfectie hebben de muizen nog geen schimmelinfectie, waardoor we geen licht waarnemen. Daarop worden ze geïnfecteerd met schimmel waarop we na drie dagen veel licht zien in de IAPA-muizen, wat op ernstige schimmelinfectie wijst. Muizen die minder of geen IFN-γ aanmaken, vertonen veel minder licht, wat wijst op een lagere hoeveelheid schimmel in hun longen. De kleuren in de beelden geven de intensiteit van het licht en dus de hoeveelheid schimmel aan: rood betekent veel schimmel, terwijl blauw aangeeft dat er weinig schimmel aanwezig is.
De kennis die we hebben opgedaan uit dierstudies kunnen we mogelijk in de toekomst toepassen bij patiënten. Enerzijds kunnen we overwegen om IFN-γ te gebruiken als merker om te beoordelen of patiënten een verhoogd risico lopen op het ontwikkelen van een schimmelinfectie. Op basis daarvan kunnen we dan overwegen om deze patiënten zeer gericht te behandelen met cytokine-manipulatoren die het teveel aan IFN-γ kunnen verlagen. Toekomstige klinische studies zullen moeten uitwijzen of deze benadering patiënten met IAPA een gunstiger vooruitzicht kan bieden.
We hebben een eerste belangrijke stap in de goede richting gezet, maar de weg naar het gebruik van immunotherapie in IAPA is nog lang en meer onderzoek is nodig om de volledige immunologische code te ontcijferen om zo nieuwe therapieën te ontwikkelen, te testen en te valideren in patiënten met IAPA. Dit onderzoek is dringend, omdat het niet langer de vraag is of, maar wanneer en hoe een volgende pandemie onze wereld zal treffen met nieuwe of beter aangepaste virussen. En dan zullen we ook gewapend moeten zijn om de bijbehorende dodelijke schimmelinfectie te kunnen behandelen.
Meer weten over deze studie? Je vindt het volledige onderzoek hier.
Laura Seldeslachts schreef deze blog in samenwerking met Katrien Lagrou, Stephanie Humblet-Baron, Joost Wauters en Greetje Vande Velde.
Referenties
1 Sciensano. Sciensano influenza cijfers. https://www.sciensano.be/nl/gezondheidsonderwerpen/influenza/cijfers#:~:text=Griep in België&text=Gemiddeld worden elk jaar 500.000,550.000 op 11 miljoen inwoners).
2 Seldeslachts L, Vanderbeke L, Fremau A, et al. Early oseltamivir reduces risk for influenza-associated aspergillosis in a double-hit murine model. Virulence 2021; 12: 2493–508.
3 Seldeslachts L, Jacobs C, Tielemans B, Vanhoffelen E, Van der Sloten L, Vande Velde G. Overcome double trouble : Baloxavir Marboxil suppresses influenza thereby mitigating secondary invasive pulmonary aspergillosis. J Fungi 2021; 8:1.
4 Seldeslachts L, Staels F, Gkountzinopoulou M, et al. Damping excessive viral-induced IFN- γ rescues the impaired anti- Aspergillus host immune response in in fl uenza-associated pulmonary aspergillosis. eBioMedicine 2024; 108: 105347.




