Terwijl klassieke behandelingen van kanker tumoren rechtstreeks aanvallen, probeert immunotherapie het verdedigingssysteem van het lichaam zelf tegen kwaadaardige weefsels te stimuleren.
Het idee dat het immuunsysteem kanker in bedwang zou kunnen houden, is niet nieuw. Pogingen om het verdedigingssysteem van het eigen lichaam tegen kwaadaardige gezwellen in te zetten werden al meer dan honderd jaar geleden ondernomen. William Coley, toen als chirurg verbonden aan het New York Cancer Hospital, probeerde voor dit doel door hitte gedode bacteriën te gebruiken. Coley merkte op dat sommige patiënten langer in leven bleven nadat ze na een heelkundige ingreep waarbij een tumor werd verwijderd, een infectie ontwikkelden. Zo kwam hij tot de hypothese dat het verdedigingssysteem dat tegen de infectie werd gemobiliseerd, ook de tumor kon aanpakken.
De daaropvolgende decennia maakte onderzoek veel duidelijk over de cellen die dit beschermende systeem mogelijk maken, en ook over de chemische mediatoren en de moleculaire schakelaars die het nauwkeurig sturen. De onderzoekers kwamen erachter hoe het immuunsysteem snel wordt gemobiliseerd om potentieel gevaarlijke besmettelijke pathogenen, zoals bacteriën en virussen, te detecteren. Al even belangrijk is dat de onderzoekers gedetailleerd de vele triggers beschreven die het immuunsysteem signaleren dat het zijn respons moet matigen zodat het niet te veel gezond weefsel vernietigt. Zo verwierven ze een gedetailleerd inzicht in de manier waarop het immuunsysteem op kanker reageert en hoe het door kanker wordt beïnvloed.
Het eerste niveau van de verdediging tegen pathogenen bestaat uit een algemene respons tegen bacteriën en virussen. Die respons wordt gecoördineerd door witte bloedcellen, met name neutrofielen en monocyten. Deze cellen maken deel uit van wat we het aangeboren immuunsysteem noemen. Hun taak is bepaalde aspecten herkennen van de moleculaire anatomie die gemeenschappelijk is voor alle bacteriën en virussen – zoals delen van hun buitenste wand of afwijkingen in de structuur van hun DNA en RNA die verschillen van wat normaal in hogere organismen wordt gevonden. Hoewel deze witte bloedcellen hun aanval niet op specifieke soorten of proteïnes richten, slagen ze er toch in een groot aantal van de microbiologische indringers te vernietigen en moleculaire fragmenten te genereren – die we kennen als antigenen – die andere spelers van het immuunsysteem als vreemd waarnemen.
Het immuunsysteem zou in staat moeten zijn kwaadaardige cellen te herkennen. Toch slaagt het er om verschillende redenen vaak niet in
Cellen die verantwoordelijk zijn voor het tweede niveau van de verdediging, het adaptieve immuunsysteem, zien deze antigenen als startpunt voor een veel nauwkeuriger gerichte respons. Een respons die, als hij succesvol is, een levend geheugen vormt waarin de microbiële indringers worden opgeslagen zodat ze in de toekomst makkelijk kunnen worden vernietigd. Twee verschillende types cellen – T-cellen en B-cellen – vormen het hart van deze adaptieve respons. Er zijn diverse soorten T-cellen, maar ze stammen allemaal af van precursoren die worden aangemaakt in de thymus, een klein orgaan dat zich in het midden van de borst net boven het hart bevindt. B-cellen worden aangemaakt in het beenmerg en vormen de moleculen van antilichamen. Antilichamen en sommige moleculen op T-cellen richten zich op specifieke antigenen en maken het zo voor het immuunsysteem mogelijk op bacteriën en geïnfecteerde cellen die deze antigenen op hun oppervlak dragen, te mikken en ze te vernietigen.
Uiteraard zijn kankers geen infecties. Ze ontstaan wanneer de eigen cellen van het lichaam bepaalde genetische en andere veranderingen ondergaan. Het immuunsysteem zou eigenlijk in staat moeten zijn kwaadaardige cellen te herkennen, want ze vertonen abnormale moleculaire fragmenten die voor de T- en de B-cellen vreemd moeten lijken. Toch slaagt het er om verschillende redenen vaak niet in efficiënt tegen kankers op te treden. Al jaren wordt, met wisselend succes, getracht de respons te versterken. De recente, meer consistent succesvolle benaderingen volgen een andere weg. Nu blijkt dat kankers soms met de uitschakelmechanismen van het immuunsysteem gaan samenwerken en actief de immuunrespons tegen kwaadaardige cellen afremmen. Met de nieuwe aanpak wordt getracht deze remmen het zwijgen op te leggen.
Checken en afwegen
De experimentele medicatie die Shirley’s leven redde, past in de nieuwe zienswijze. Die vloeide voort uit onderzoek aan de proteïne CTLA-4. Die is aanwezig in veel soorten T-cellen, maar wordt alleen actief nadat bepaalde T-cellen hun doelwit hebben herkend en van andere moleculen groen licht hebben gekregen. Zodra hij geactiveerd is, werkt CTLA-4 samen met een aantal andere proteïnes als een reeks moleculaire remmen of checkpoints die het immuunsysteem beletten al te destructief te worden.
Dat deze checkpoints noodzakelijk zijn, zien we in dieren die ze niet hebben. Muizen die genetisch zo gemodificeerd zijn dat ze de CTLA-4 proteïne niet hebben, sterven drie à vier weken na hun geboorte. Omdat niets de escalatie van de immuunrespons een halt toeroept, infiltreren geactiveerde T-cellen alle organen in het lichaam. De organen worden volledig vernietigd. Deze ontdekking, gepubliceerd in 1995, toonde aan dat een permanent ontbreken van deze ene molecule tot een destructieve auto-immuunreactie kan leiden.
Datzelfde jaar formuleerde James Allison, toen verbonden aan de Universiteit van California, Berkeley, de hypothese dat als de moleculaire rem CTLA-4 tijdelijk kon worden uitgeschakeld, het immuunsysteem in staat zou zijn een krachtiger aanval tegen kankercellen in gang te zetten en zo tumoren zou kunnen verkleinen. Allison en zijn collega’s wilden de hypothese testen door in muizen een synthetisch ontwikkeld antilichaam in te brengen dat de activiteit van CTLA-4 blokkeert.
Voor een groot aantal tumoren wordt immunotherapie wellicht een mogelijke behandeling, naast chemo- en radiotherapie
Het was duidelijk dat het blokkeren van CTLA-4 resulteerde in de regressie van verscheidene types tumoren – waaronder darmkanker en sarcoom – die in de proefdieren waren getransplanteerd. Bij andere proeven bleek dat melanomen aanzienlijk kleiner werden wanneer muizen waren behandeld met het CTLA-4 blokkerende antilichaam en met een experimenteel vaccin – gemaakt van gemodificeerde melanoomcellen – dat was ontwikkeld om een specifiek op die kanker gerichte immuunaanval uit te lokken.
De volgende stap bestond erin deze benadering, technisch omschreven als het immunologisch blokkeren van een checkpoint, op mensen toe te passen. Allison vond daarvoor een bereidwillige partner in het biotechnologische bedrijf Medarex, dat in handen is van het farmaceutische bedrijf Bristol Myers Squibb. Dat ontwikkelde een volkomen menselijke versie van een DTLA-4 blokkerend antilichaam (aanvankelijk MDX-010 genoemd en nu bekend als ipilimumab). Allison begon klinische tests met patiënten met ver gevorderde kankers die niet op andere therapieën reageerden.
Al van bij de eerste test, en later ook bij erop volgende, werd bij een aantal patiënten een duidelijke regressie van de tumoren vastgesteld. Toch bleek dat andere tests niet tot dezelfde resultaten leidden. De onderzoekers leerden dat wat immunotherapie betreft de klassieke manier om na te gaan of een behandeling van kanker al dan niet succesvol is, misleidend kan zijn.
Succes meten
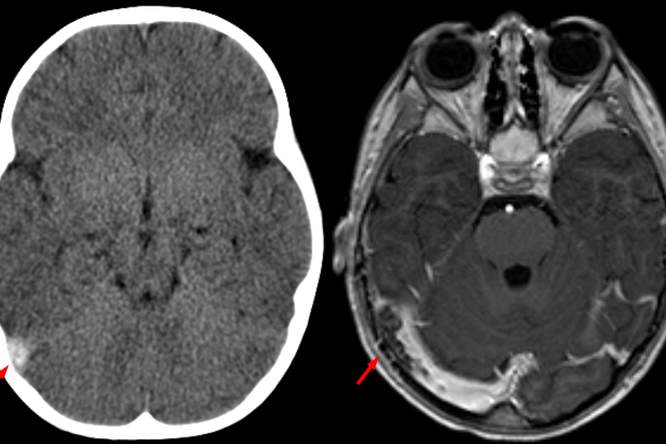
Oncologen kunnen meestal redelijk snel zeggen hoe goed een patiënt op een klassieke behandeling van kanker reageert. We gebruiken daarvoor medische beeldvormingstechnologie – CT-scans (computertomografie), PET-scans (positronemissietomografie) of MR-scans (beeldvorming door magnetische resonantie). Met die technieken registreren we de grootte van een tumor net voor de behandeling start en ongeveer zes weken later. Als de groei van de kwaadaardige gezwellen significant trager gaat verlopen, dan kunnen we de behandeling verder zetten omdat ze effect lijkt te hebben. Als dat niet zo is, dan kunnen we een alternatieve behandeling overwegen of de behandeling stopzetten.
Bij het toepassen van immunotherapie is het nemen van dergelijke beslissingen niet zo eenvoudig. In de eerste plaats moeten we het immuunsysteem meer tijd gunnen om geactiveerd te raken. Daarom wordt een tweede meting van de grootte van de tumor pas twaalf weken na het starten van de behandeling uitgevoerd. Zelfs als we rekening houden met de zes extra weken van observatie en behandeling, bleken de resultaten van de tests met het blokkeren van CTLA-4 verwarrend. De scans van sommige patiënten lieten een duidelijke verbetering zien, terwijl die van anderen lieten zien dat al bestaande tumoren groter waren geworden of zelfs dat nieuwe tumoren waren ontstaan. En toch voelden sommige patiënten met groter geworden tumoren zich beter.
We zien nu twee mogelijke verklaringen voor het feit dat tumoren na immunotherapie groter kunnen worden: ofwel werkt de behandeling niet, ofwel werd de kwaadaardige groei door een groot aantal T-cellen of andere immuuncellen versterkt. Met andere woorden, grotere tumoren kunnen er – paradoxaal genoeg – op wijzen dat de behandeling wel degelijk werkt: we moeten alleen wat langer wachten om de groei te zien afnemen. Aangezien het zo moeilijk is om de vooruitgang tijdens immunotherapie te meten, gebruiken onderzoekers die de werking van ipilimumab testen nu het eenvoudige en belangrijke assessment van de tijd dat de patiënten nog in leven blijven. Voor hun analyses blijkt dit het meest geschikte eindpunt.
Resultaten van de meest recente klinische studies tonen aan dat iets meer dan twintig procent van de patiënten met metastatisch melanoom die met ipilimumab zijn behandeld, de ziekte langere tijd onder controle houden en na het starten van de behandeling langer dan drie jaar in leven blijven. Dit is een belangrijk gegeven, want vóór nieuwe medicijnen als ipilimumab ontwikkeld waren, was de gemiddelde levensverwachting voor patiënten met metastatisch melanoom zeven tot acht maanden. Sommige van de eerste patiënten die het middel kregen toegediend, zoals Shirley, leven sinds het starten van de behandeling nu al langer dan vijf jaar.
Intussen schoot ook het onderzoek aan PD-1 op, een tweede molecule die het immuunsysteem afremt. PD-1 bevindt zich op het oppervlak van tal van T-cellen. Wanneer ze aan bepaalde andere moleculen wordt gebonden, dan dwingt PD-1 de cellen waarop de molecule zich bevindt, zichzelf te vernietigen – een normaal proces dat, zoals bij de nauw verwante proteïne CTLA-4, ervoor zorgt dat een aan gang zijnde immuunreactie op veilige wijze wordt stopgezet. Sommige tumorcellen zijn echter zo geëvolueerd dat ze om zichzelf te verdedigen hun oppervlak bedekken met moleculen die de PD-1 proteïnes op T-cellen misleiden, en het proces van zelfvernietiging te snel in gang zetten. Het resultaat daarvan is dat elke T-cel die een kankercel aanvalt, een signaal krijgt om in de plaats daarvan zichzelf te vernietigen. Dit treffende voorbeeld is er slechts één van de vele manieren waarop tumoren het immuunsysteem kunnen beletten efficiënt te werken.
(klik op de afbeelding om ze groter te bekijken)
Medicijn
De farmaceutische bedrijven Merck, MedImmune en Genentech hebben elk antilichamen ontwikkeld die voorkomen dat diverse soorten tumoren PD-1 er toe aanzetten T-cellen tot zelfdoding dwingen. Uit recente klinische tests blijkt dat deze experimentele stoffen bij meer dan dertig procent van de patiënten met melanoom leiden tot lange periodes van remissie, soms zelfs jarenlang. Dat geldt ook voor een klein aantal patiënten voor wie een eerdere behandeling met ipilimumab niet effectief was gebleken. Verscheidene van mijn collega's van Memorial Sloan Kettering en medewerkers van heel wat andere onderzoekscentra testten de PD-1 blokkerende middelen bij patiënten met een bepaald type longkanker. Bij meer dan twintig procent van de deelnemers aan dat onderzoek is langdurige regressie waargenomen.
De resultaten bij longkanker, die werden gerapporteerd in november 2013, lijken voor de immunotherapie een belangrijk keerpunt te vormen. Sceptische clinici kunnen nu niet langer volhouden dat de nieuwe benadering alleen zinvol is voor een beperkt aantal specifieke soorten tumoren, zoals melanoom en nierkanker. Beide vormen bleken eerder al bijzonder gevoelig voor behandelingen op basis van immuuntherapie. Die therapie blijkt nu ook tegen een breder gamma van kankers te werken. Het is niet onwaarschijnlijk dat voor een groot aantal tumoren de nieuwe benadering snel aan chemotherapie en radiotherapie zal worden toegevoegd.
Zoals bij de meeste behandelingen van kanker het geval is, is ook bij immunotherapie sprake van een aantal neveneffecten. Zo kunnen bijvoorbeeld patiënten die anti-CTLA-4 medicatie krijgen, ontstekingsreacties op de huid en in de dikke darm vertonen. Die ontstaan wanneer immuuncellen te veel prikkelende chemische stoffen vrijgeven. De hieruit resulterende huiduitslag en pijnlijke krampen en diarree worden standaard behandeld met immuunsysteem onderdrukkende steroïden, zoals bijvoorbeeld prednison. Ook patiënten die een therapie volgen om de werking van PD-1 te blokkeren, kunnen met dit soort opstoten te maken krijgen – vooral in de nieren, de longen en de lever – maar die zijn doorgaans minder frequent en minder krachtig dan bij het blokkeren van CTLA-4. Gelukkig is het zo dat door het toedienen van ontstekingsremmers het therapeutische effect van beide middelen niet wordt onderdrukt.
Naar genezing van kanker?
Ontstekingen kunnen wel tot ernstiger problemen leiden. Lange tijd maakten onderzoekers zich zorgen over het feit dat de prikkelende cascade kan leiden tot bijzonder krachtige auto-immuunreacties, waarbij het immuunsysteem steeds grotere hoeveelheden gezond weefsel aanvalt en vernietigt. In tegenstelling tot een echte auto-immuunziekte blijken deze neveneffecten van de ontstekingen echter van voorbijgaande aard en komen ze na behandeling niet meer terug.
Omdat antilichamen tegen PD-1 en CTLA-4 de immuunrespons tegen tumoren op verschillende manieren een boost lijkt te geven, is het zinvol te onderzoeken of het gelijktijdig toedienen van de middelen veilig en efficiënt kan zijn. In 2007 toonden experimenten op proefdieren met darmkanker en melanoom aan dat het gecombineerd blokkeren van CTLA-4 en PD-1 efficiënter is dan het apart toedienen van beide middelen. Daarom besliste mijn onderzoeksgroep in 2010, samen met Mario Sznol van Yale University, een klein veiligheidsonderzoek te starten naar het gebruik van ipilimumab en het PD-1 blokkerende middel nivolumab bij 53 patiënten met metastatisch melanoom.
Alles bij elkaar geloof ik dat het eindelijk tijd is om realistisch te beginnen denken aan langdurige remissies, zelfs aan genezing
De onderzoeksresultaten, die we vorig jaar op een medische conferentie presenteerden, waren indrukwekkend. Bij meer dan vijftig procent van de patiënten die we hadden behandeld met wat wij als de optimale doses van de antilichamen beschouwden, waren de tumoren met meer dan de helft van hun oorspronkelijke grootte verkleind. Deze reacties verschillen dramatisch van deze die worden bereikt als de middelen apart worden toegediend. Neveneffecten traden vaker op dan bij een aparte toediening, maar bleken, net zoals tevoren al het geval was, goed met corticosteroïden controleerbaar. Het is wel belangrijk hier te benadrukken dat deze vroege resultaten het gevolg zijn van een onderzoek met een beperkt aantal patiënten, en dat bij een uitgebreider of langer durend onderzoek de resultaten misschien niet zo gunstig zijn. Momenteel loopt een uitgebreider onderzoek van het gecombineerd blokkeren met ipilimumab en nivolumab bij meer dan negenhonderd patiënten met een melanoom.
Andere clinici onderzoeken deze gecombineerde immunotherapie voor het behandelen van longkanker, nierkanker, maagkanker, borstkanker, hoofd- en halskanker en alvleesklierkanker. Het is ook mogelijk dat het tegelijkertijd uitvoeren van directe aanvallen op de tumor – samen met chemotherapie of radiotherapie – immunotherapie nog effectiever maakt als de kankercellen afsterven op een manier die het aangeboren deel van het immuunsysteem triggert. Het resultaat kan een perfecte therapeutische ‘storm’ zijn die tumorcellen vernietigt en het mogelijk maakt het puin beter door het immuunsysteem te laten herkennen. Zo'n combinatie zou ook de vorming van het geheugen van de T-cellen kunnen versterken, zodat die, lang nadat de behandeling werd afgesloten, waakzamer blijven voor het ontstaan van nieuw kwaadaardig weefsel. Of deze vorm van immunotherapie voor een potentieel groter effect met andere types van immunotherapie die momenteel worden ontwikkeld – zoals vaccins tegen kanker – moet worden gecombineerd, is nu nog niet duidelijk.
Alles bij elkaar geloof ik dat het eindelijk tijd is om realistisch te beginnen denken aan langdurige remissies, zelfs aan genezing. We kunnen nu immers standaardbehandelingen die zich rechtstreeks op de tumor richten, combineren met immunotherapieën die het verweer van de patiënt zelf een boost geven.
Dit artikel verscheen in Eos magazine, nummer 5, 2014.