Met prime editing richt onderzoeker Mattijs Bulcaen zich op een levensbedreigende aandoening: mucoviscidose of taaislijmziekte. Hoe werkt die 'moleculaire typemachine'?
Beeld: © KU Leuven – Rob Stevens
September 2020 – Terwijl het land kopje onder gaat in de tweede coronagolf, fiets ik in een rotvaart Gasthuisberg op. Geen tijd te verliezen, want vandaag wordt een heel spannend experiment uitgelezen. In de vroege stilte flikkeren de labo-armaturen aan en hul ik mezelf in een lange overjas, labobril en blauwe handschoenen. Helemaal alleen in een donker kamertje schuif ik twee plaatjes onder de microscoop. Prachtige cellen verschijnen onder het objectief. Op basis van een visuele vergelijking lijken de plaatjes identiek. De cellen zien er gelukkig en vredig uit. Tijd om ze uit hun zalige rust te halen en aan een grondigere analyse te onderwerpen. Een hele dag ben ik in de weer om het DNA uit de cellen op te zuiveren. Tegen de avond snel ik met klein zakje naar een postbus gemonteerd bij een ander KU Leuven labo. Enkele minuten later worden de stalen opgehaald en richting Berlijn gevoerd.
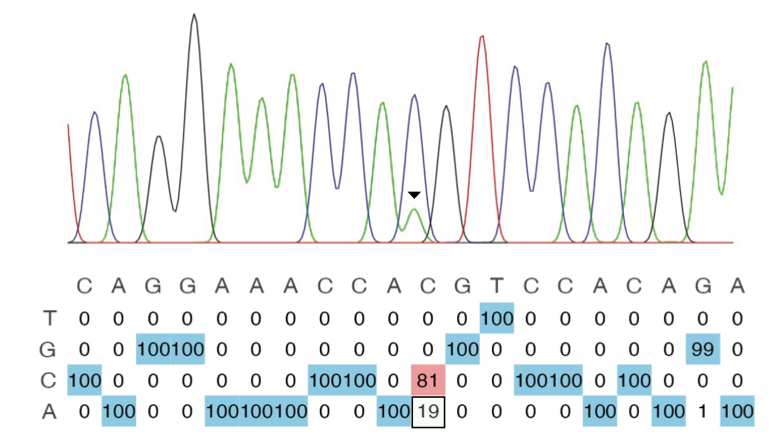
Het vonnis arriveert twee dagen later als een bestand met piekjes. Nerveus en ongeduldig tuur ik tussen honderden piekjes tot plots … EUREKA! Op één van de posities bespeur ik een heel klein tweede piekje. Noem het een baby-piek. Meer dan een jaar al was ik hiernaar opzoek. In een euforische opwelling stuur ik “what may appear a little hump might become something great” naar mijn collega’s. Het kleine piekje wordt de aanzet van vier jaar onderzoek in het laboratorium voor Moleculaire Virologie en Gentherapie van professoren Zeger Debyser en Marianne Carlon.
Maar wat zat nu in dat piekje? Welnu, de piekjes tonen de resultaten van zogenaamde sequencing data, oftewel uitgelezen DNA code. Wat ik hier in 2020 waarnam, was een eerste precieze correctie van het CFTR gen. Het zou de kern van mijn onderzoek worden en de deur tot nog veel belangrijkere resultaten.
Muco
De groep van prof. Carlon aan de KU Leuven zoekt al meer dan tien jaar naar oplossingen voor mucoviscidose (muco) ofwel taaislijmziekte. Muco is in Europa de meest voorkomende levensbedreigende erfelijke aandoening. De ziekte wordt veroorzaakt door foutjes in het CFTR gen. Dat is een stuk DNA dat de instructies bevat voor een essentieel zoutkanaaltje. Mensen met aangeboren afwijkingen in het CFTR gen maken ofwel geen ofwel gebroken zoutkanaaltjes. Als gevolg ontwikkelt zich een ongeneeslijke longziekte. De zoutkanaaltjes zijn belangrijk om slijmlaagjes in verschillende organen vochtig te houden. Indien dat niet gebeurt, stapelen dikke proppen taai slijm zich op. Dat leidt tot moeilijkheden om te ademen en veroorzaakt ook chronische infecties. Muco is een complexe aandoening. De behandeling vergt de expertise van verschillende takken van de geneeskunde. De moleculaire oorzaak van alle symptomen is echter opmerkelijk simpel: één of enkele foute lettertjes in het DNA. Miljoenen euro’s en dollars werden reeds uitgegeven aan de zoektocht naar oplossingen voor muco. Die investeringen hebben zeker wel gerendeerd, maar tot nog toe was niemand in staat om de oorzaak aan te pakken. Niemand was in staat om die ene DNA letter om te draaien naar de juiste.
Knippen en plakken met DNA: easy toch?
Die opdracht lijkt nochtans niet zo moeilijk. In een Word-document is de klus in een paar seconden geklaard. Control + F om het foutieve woord op te sporen en daarna gewoon de correctie intypen. Helaas (of gelukkig?) zijn levende wezens echter geen Word-documenten. De “code” die op ons DNA ligt opgeslagen bestaat niet écht uit lettertjes. Onze genetische code is een complexe ketting van aaneengeschakelde biochemische moleculen. Hoewel deze wel aangeduid worden als A, C, T en G, zijn ze helemaal niet zo makkelijk te lezen of bewerken. Om van een A een G, te maken bijvoorbeeld, moet een complexe zijgroep van de molecule veranderd worden. Om een letter in te voegen, moet de ketting geopend worden, moet een molecule bijgeplaatst worden en moet de keten daarna terug precies aan elkaar gezet worden. Bedenk ook dat een fout vinden helemaal niet makkelijk is. De menselijke chromosomen bevatten meer dan 6 miljard letters verzameld op 46 chromosomen. De opdracht komt overeen met het precies verwisselen van één enkele korrel in een gigantische zandbak. En liefst doen we dat zonder de andere zandkorrels aan te raken of te verstoren.
Prime editing geneest muco in het lab
Wat ik in 2020 voor het eerst testte in het lab in Leuven was “prime editing”. Een op dat moment splinternieuwe techniek om gericht aanpassingen te maken in DNA. We maakten hiervoor gebruik van eiwitten die in de natuur evolueerden om DNA te kunnen binden en aanpassen. We programmeerden deze eiwitten om de muco-letter te verwijderen en precies aan te passen. Prime editing bouwt verder op de revolutionaire CRISPR-Cas techniek, maar is nog een stuk krachtiger. Twee zaken maken de prime editing technologie bijzonder interessant. Ten eerste is het mogelijk om specifiek te kiezen waar de eiwitten gaan binden in het DNA. Die zoekfunctie wordt vervolgens gecombineerd met een module die omschreven kan worden als een “DNA-typemachine”. De prime editing eiwitten zullen zo eerst de juiste plek in het DNA zoeken om vervolgens een chemische molecule te veranderen of aan te hechten. Uitwissen en herschrijven, maar dan op moleculair niveau. Na het eerste succesje in 2020, optimaliseerden we de techniek. Tegen 2021 waren we in staat om cellen van mensen met muco te genezen in het lab.
Levende balonnetjes – humane organoïden
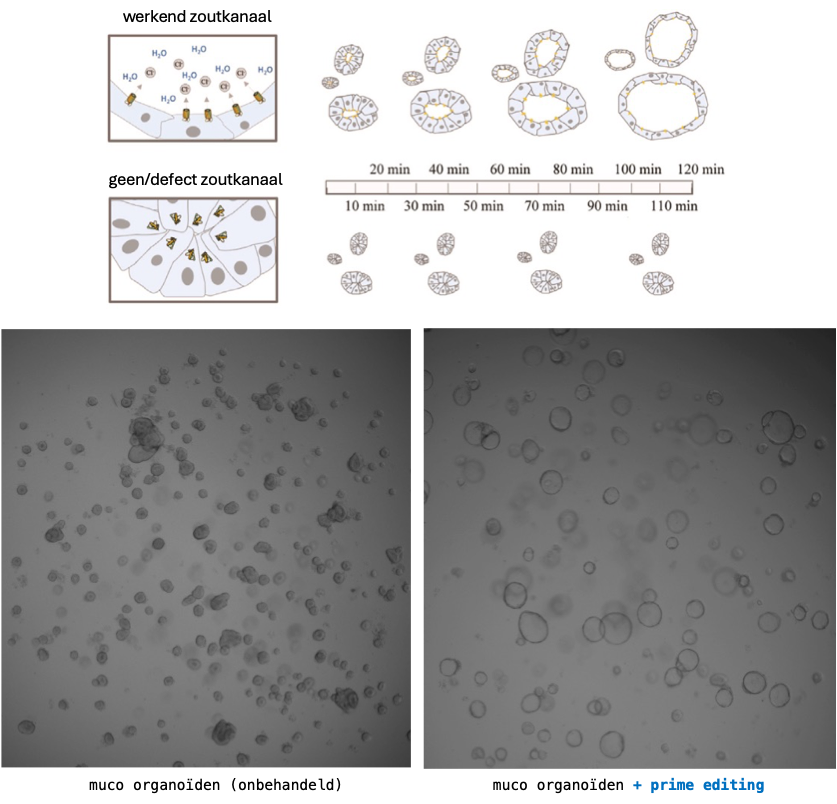
Een populaire manier in het muco-veld om nieuwe therapieën te testen zijn organoïden. Deze bolvormige “minidarmpjes” worden in het lab opgegroeid vanuit cellen gedoneerd door mensen met muco. Organoïden van mensen zonder muco beginnen al snel spontaan op te blazen als kleine organische ballonnetjes. Bij organoïden van mucopatiënten is die reactie geheel afwezig. Het verschil kan teruggebracht worden tot het zoutkanaaltje. Het pompen van zout naar de binnenkant van de sferische structuur trekt water aan. Dat doet de organoïden zwellen door osmose. Organoïden van mensen met muco ontbreken het zoutkanaaltje echter en kunnen niet zwellen. Het is een zwart-wit situatie. Zwellen of niet. Werkend zoutkanaaltje of niet. Muco of geen muco.
Na eerste testbehandeling in 2021 zagen we een paar zwellende organoïden verschijnen in een muco-staal. Een voorzichtige start, maar toch heel bemoedigend. De persoon die deze cellen doneerde had en heeft nog steeds muco, maar hier in het lab, op kleine schaal, konden we zijn of haar cellen genezen. Genetische analyse toonde later ook aan dat het DNA in de cellen ook effectief gecorrigeerd was. Ondertussen worden in het lab van professor Carlon al veel hogere efficiënties behaald.
Hoe moet het verder?
De resultaten van ons onderzoek werden in mei gepubliceerd in het respectabele vakblad “Cell Reports Medicine”. Het werk toont aan dat spellingscorrectie op chromosomen niet langer science fiction is. Verder toonden we ook aan dat in luchtwegcellen, correctie van slechts een heel klein percentage aan cellen (1.5%) genoeg kan zijn om voldoende zoutkanaal activiteit te bekomen. Da’s belangrijk want de longen bestrijken een enorm oppervlakte aan cellen. Ze allemaal corrigeren zou heel moeilijk zijn. We bewezen ook dat de genmodificatie veilig was. In grondige analyses konden we geen zogenaamde “off-target hits” vinden, met andere woorden, prime editing veranderde geen DNA lettertjes ergens anders in het humane genoom. Is onze muco-behandeling nu klaar om bij mensen toe te dienen? Nog niet onmiddellijk. Daarvoor moet eerst nog een goed vervoermiddel gevonden worden. Prime editing is een heel geavanceerde technologie en kan niet zomaar in een pilletje gegeven worden. In het Carlon lab, maar ook over de hele wereld zijn wetenschappers op zoek naar goede vervoersmiddelen voor dit soort technologie. Er is nog veel werk aan de winkel, maar we zijn hoopvol en blijven doorduwen.
De wetenschappelijke publicatie van het onderzoek vind je via deze link: Bulcaen et al., Cell Reports Medicine, 2024




