Het onderzoek naar de ziekte van Alzheimer heeft een probleem. Wezenlijke vooruitgang voor patiënten is er de afgelopen decennia niet geboekt. Hoe komt dat?
Alzheimeronderzoek en nieuwe medicijnen tegen de ziekte halen geregeld het nieuws. Deze week werd het nieuwe medicijn donanemab gepresenteerd, dat de ontwikkeling van alzheimer licht afremt. Ondanks grote onderzoeksbudgetten is er nog steeds geen echte behandeling voor alzheimerpatiënten. Hoe komt dat? Je leest het in dit artikel, dat afgelopen april in Eos verscheen.
Er zijn duizenden onderzoekers werkzaam op het gebied van alzheimer. Er zijn tijdschriften en congressen die er speciaal aan zijn gewijd. Overheden en particuliere fondsen besteden er jaarlijks miljarden aan. Maar in al de decennia dat het onderzoek inmiddels loopt, is een behandeling voor alzheimerpatiënten niet dichterbij gekomen. Over de oorzaken van de aandoening heerst geen eenstemmigheid en wezenlijke vooruitgang is niet geboekt. Dat wil zeggen, het onderzoek heeft natuurlijk allerlei nieuwe kennis over de hersenen opgeleverd, maar niets waar patiënten veel aan hebben.
Als we cynisch zijn, kunnen we zeggen dat alzheimer voor de biomedische wereld een uitstekend verdienmodel is. Het gaat om een aandoening waar een groot deel van de westerse bevolking mee te maken krijgt, als patiënt, familielid of verzorger. Wie met alzheimerpatiënten te maken krijgt, wordt snel overtuigd van de noodzaak om een oplossing te vinden. Met de toename van de levensverwachting en de vergrijzing van de bevolking legt de verzorging van alzheimerpatiënten bovendien een steeds grotere druk op de gezondheidszorg. De noodzaak om iets te doen is zonneklaar. Vandaar dat de overheid en wetenschappelijke instellingen weinig aansporing nodig hebben om diep in de buidel te tasten.
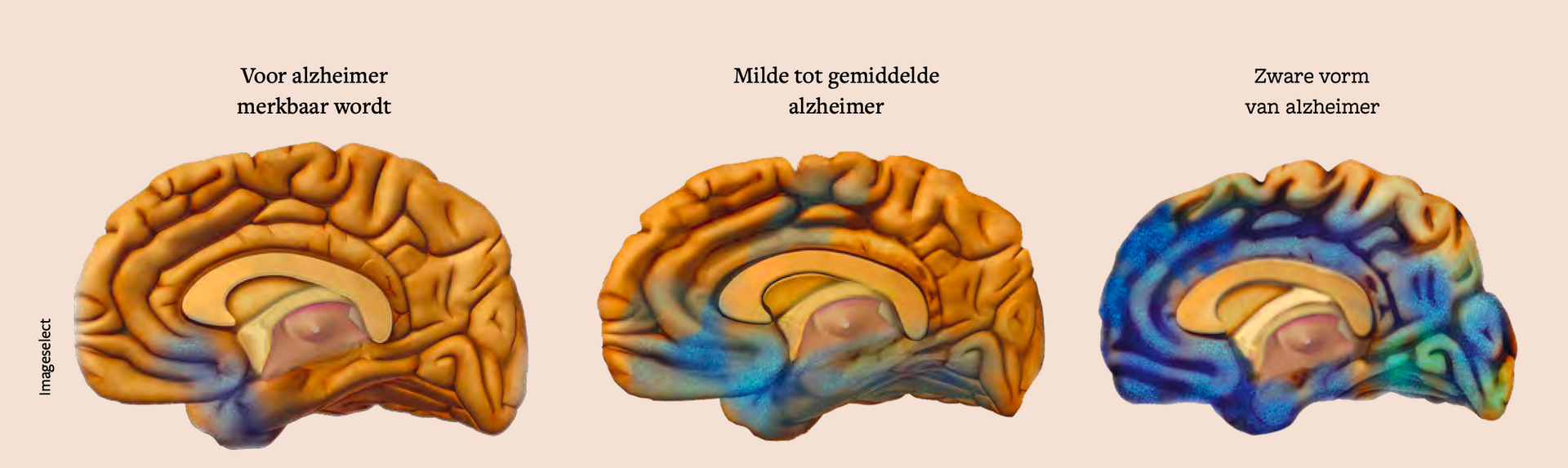
Het eiwit bèta-amyloïde zou aanzetten tot de vorming van tangles, het verstoren van de functies van zenuwcellen in de hersenen, en uiteindelijk tot het afsterven van deze cellen.
Alleen, dan blijkt dat dat allemaal weinig oplevert. Treurig voor de patiënten en hun familieleden, maar zo zoetjesaan ook behoorlijk gênant voor de onderzoekers. Dit dwingt tot zelfonderzoek. Hoe is het zover gekomen en is de huidige aanpak wel de juiste?
Historici over wetenschappelijk onderzoek
Alzheimeronderzoekers realiseren zich inmiddels dat er problemen op een dieper niveau spelen, maar de manier waarop ze daarover spreken blijkt bij nader inzien niet altijd heel vruchtbaar. Dat is onlangs aangetoond door twee Nederlandse wetenschapshistorici, Noortje Jacobs uit Rotterdam en Bert Theunissen uit Utrecht, die als buitenstaanders keken wat er vanuit hun vak over het alzheimeronderzoek valt te zeggen. Daarbij konden ze terugvallen op het begrippenapparaat waarmee historici wetenschappelijke ontwikkelingen en discussies plegen te analyseren. Hun bijdrage verscheen niet in een wetenschapshistorisch tijdschrift, maar werd gepubliceerd als een editorial in het prominente Journal of Alzheimer’s Disease. Het is duidelijk, ook de alzheimeronderzoekers zelf voelen inmiddels de behoefte aan een kritische blik van buiten. Hun analyse leidt tot enkele leerzame conclusies.
Eerst een beetje geschiedenis. Het onderzoek naar alzheimer wordt al sinds jaren gedomineerd door de zogenaamde amyloïdecascadehypothese, voor het eerst geformuleerd in 1992. Het was al sinds de jaren 1930 bekend dat sommige patiënten die leden aan ernstige geestelijke aftakeling na hun overlijden zogenaamde plaques (een neerslag van eiwitten die de communicatie tussen de hersencellen moeizamer maakt, red.) en tangles (samenklonterende eiwitten die een kluwen vormen) in hun hersenen bleken te hebben. Het lag voor de hand een verband te zien met hun aandoening. In 1992 formuleerden twee Amerikaanse onderzoekers een hypothese volgens welke een bepaald eiwit, kort aangeduid als bèta-amyloïde, een hoofdbestanddeel van de plaques, de hoofdschuldige was. Via een keten van reacties zou dit eiwit aanzetten tot de vorming van tangles, het verstoren van de functies van zenuwcellen in de hersenen, en uiteindelijk tot het afsterven van zenuwcellen. Hoe deze reacties precies verliepen, zou nader moeten worden uitgezocht.
De hypothese initieerde daarmee een duidelijk onderzoeksprogramma. Dat programma bood uitzicht op een verklaring van de ziekte en uiteindelijk, als het mechanisme eenmaal ontrafeld zou zijn, op middelen om er tegen op te treden. Het is dan ook vanaf 1992 dat de geldkraan voor onderzoek naar de ziekte van Alzheimer wijd werd opengezet. De gezamenlijke stootkracht van al die onderzoekers moest het probleem snel oplossen.
Alleen, zo ver kwam het niet. Het veronderstelde mechanisme bleef de onderzoekers ontgaan. Daarnaast waren er ook allerlei feiten die in strijd leken met de hypothese. Niet alle patiënten met plaques in hun hersenen ontwikkelen de ziekte van Alzheimer, en bij sommige patiënten is niets afwijkends in hun hersenen te vinden. Dat betekent niet noodzakelijk dat de hypothese onjuist is, maar er is kennelijk wel meer aan de hand dan het simpele model aangeeft. Er bleven dan ook altijd dissidenten die de hypothese afwezen en met andere ideeën kwamen. Het veld was inmiddels zo groot dat er ruimte was voor iedereen. Alleen kon geen van de alternatieve ideeën collega-onderzoekers erg enthousiast maken.
Wetenschappelijke loopgravenoorlog
Nu concrete resultaten uitblijven, wat is de situatie voor alzheimeronderzoekers? Hoe rechtvaardigen zij de enorme bedragen die jaarlijks aan hun onderzoek besteed worden? Voelen zij de behoefte om het roer om te gooien of willen zij juist stug volhouden op het ingeslagen pad? Dat er inderdaad behoefte is aan zelfonderzoek blijkt uit de manier waarop de discussies in het veld inmiddels worden gevoerd. Het gaat niet meer enkel om de precieze interpretatie van concrete experimenten, maar ook om wat eigenlijk goede wetenschap is. Dit debat wordt vooral gevoerd tussen de voor- en de tegenstanders van de genoemde amyloïdecascadehypothese. De eerste openlijke kritiek op de hypothese werd geuit in de jaren 1990. Aanvankelijk was deze kritiek hoffelijk van toon, zoals je zou verwachten in een wetenschappelijk debat. Allengs werd de toon echter scherper en in de eerste jaren van de eenentwintigste eeuw ontaardde dit in een waar moddergevecht.
De critici verweten de aanhangers van de hypothese niet minder dan onwetenschappelijk gedrag. In strijd met alle concrete bewijzen bleven zij immers stug vasthouden aan een achterhaalde theorie. De critici betitelden hun tegenstanders als gelovigen en dogmatici, vergelijkbaar met de mensen die weigerden door Galileo’s telescoop te kijken of die alle bewijs dat de aarde draait verwierpen omdat Aristoteles nu eenmaal voor eeuwig had vastgesteld dat zij stil stond. Er vielen termen als Church of Holy Amyloid en zelfs de heksenprocessen werden erbij gehaald.
De aanhangers van de hypothese lieten zich dat natuurlijk niet zeggen. Zij beschuldigden juist hun opponenten van een onwetenschappelijke houding. Met een beroep op de wetenschapsfilosoof Thomas Kuhn betoogden zij dat men in de wetenschap dient vast te houden aan bestaande theorieën tot er een betere verklaring voorhanden is. Zolang er geen fatsoenlijk alternatief is voor de amyloïdecascadehypothese (en die is er niet) is het dus onwetenschappelijk om die bij het oud vuil te zetten. Kortom, het debat wordt niet gevoerd met feitelijke, dan wel met filosofische en historische argumenten. Je kunt je voorstellen dat Jacobs en Theunissen, professionele wetenschapshistorici, geregeld hun hoofd hebben moeten schudden over dit gebruik, of eigenlijk misbruik, van de geschiedenis.
Wetenschap in crisis
Dit soort discussies – boundary discussions zoals ze in vakjargon worden genoemd – zijn typisch voor een wetenschapsgebied in crisis. Normaal bestaat over zulke kwesties geen verschil van mening. Wetenschappers sleutelen aan bepaalde deelproblemen waarvan iedereen in het veld de relevantie erkent. Met de diepere filosofische vragen daarachter houden zij zich niet bezig. Maar in een veld dat stagneert of waarvan niet duidelijk is waar het heen moet, gaan ze zich de vraag stellen wat er mis is en dan wordt het verleidelijk de schuld te leggen bij de methode zelf — dat wil zeggen, de methodes die worden toegepast door anderen dan jezelf.
Het alzheimeronderzoek is een kolossaal apparaat geworden waar enorme bedragen in omgaan en het ligt in de aard van zulke apparaten dat ze streven naar zelfbehoud
Buitengewoon vruchtbaar is deze manier van discussiëren echter niet. Jacobs en Theunissen geven hun artikel ironisch de titel ‘It’s groundhog day!’, naar de film Groundhog Day uit 1993 waarin de hoofdpersoon elke dag opnieuw wakker wordt om steeds weer in dezelfde situatie te belanden en precies dezelfde reeks handelingen te volbrengen. Op dezelfde manier bewegen de alzheimeronderzoekers inmiddels in een kringetje. Elk nieuw onderzoeksresultaat, ongeacht wat het is, bevestigt de aanhangers van beide partijen alleen maar in hun eigen gelijk en stijft hen in het vasthouden aan hun overtuiging. Hun ‘zelfreflectie’ levert al jaren steeds weer dezelfde argumenten op. De discussie is inmiddels volledig vastgelopen en langs deze weg zal het onderzoek duidelijk niet uit het slop komen.
Je zou verwachten dat de normale mechanismes die wetenschappelijke integriteit bewaken en het wetenschappelijke bedrijf vooruithelpen, zoals intercollegiale toetsing, hier reinigend zouden moeten werken. Zulke mechanismes zijn echter niet ontworpen voor een situatie als de onderhavige. Zoals de term al aangeeft, bij intercollegiale toetsing beoordelen onderzoekers uit hetzelfde vakgebied elkaars werk. Dat kan natuurlijk alleen op basis van overeenstemming over de uitgangspunten en dat is hier nu juist het probleem: de vraag is of die uitgangspunten wel houdbaar zijn. Die vraag zal bij peerreview niet snel worden gesteld. Onderzoekers gaan niet de poten onder hun eigen stoel wegzagen. Het alzheimeronderzoek is bovendien inmiddels een kolossaal apparaat geworden waar enorme bedragen in omgaan en het ligt in de aard van zulke apparaten dat ze streven naar zelfbehoud.
Is alzheimer een ziekte?
Als we de uitgangspunten van het alzheimeronderzoek tegen het licht willen houden, moeten we niet enkel kijken naar de stand van de wetenschap. Zulke uitgangspunten worden mede bepaald door allerlei politieke en maatschappelijke aspecten. Geld speelt daarin een hoofdrol. Het zijn de politiek en allerlei maatschappelijke organisaties die het alzheimeronderzoek financieren en daarmee op de been brengen en houden, maar dat doen ze alleen als ze daarmee hun eigen doelstellingen dichterbij denken te kunnen brengen.
Toen de Duitse neuropatholoog en psychiater Alois Alzheimer in 1907 het eerste geval beschreef van de aandoening die zijn naam zou krijgen, ging het om een persoon die op zijn 55ste was gestorven. Dat iemand al zo jong volledig geestelijk was afgetakeld, was duidelijk abnormaal en vroeg om een verklaring. Maar dat mensen op hoge leeftijd geestelijk en lichamelijk aftakelden, sommigen meer en anderen minder, werd indertijd als een gewoon ouderdomsverschijnsel gezien en zeker niet als een ziekte.
Geen enkele overheid steekt echter miljarden in het onderzoek naar seniele aftakeling. Zolang wat we nu alzheimer noemen werd beschouwd als een normaal ouderdomsverschijnsel was er weinig kans op ruimhartige ondersteuning van onderzoek ernaar. Dat gebeurde pas toen alzheimer werd gedefinieerd als een ziekte, dat wil zeggen, iets dat op zichzelf gezonde mensen van buiten overvalt en daarmee in principe te voorkomen of te genezen is. De amyloïdecascadehypothese werd mede daarom zo geestdriftig ontvangen omdat ze deze vooronderstelling leek te bevestigen.
Toenmalige onderzoekers speelden daar verder op in door alzheimer niet enkel voor te stellen als een ziekte, maar als een ziekte die wijdverbreid is. Dat alzheimer ouderdomsgerelateerd is, viel niet te ontkennen, maar ook bij oude mensen moest het als een te behandelen ziekte worden beschouwd. En aangezien die ziekte vanwege onze steeds langere levensduur alleen maar vaker zal voorkomen, lag hier een majeur probleem van openbare gezondheidszorg. Dit was op zich geen onredelijk idee en ongetwijfeld geloofden de betreffende onderzoekers hier oprecht in. Het probleem is dat door de mechanismen van financiering en beoordeling deze benadering vervolgens alle andere benaderingen uit de markt drukte.
Het is vaker opgemerkt dat de manier waarop het medisch onderzoek in onze wereld is georganiseerd en wordt betaald, bepaalde perverse trekjes heeft. Behandelingen voor eenvoudige en veelvoorkomende ziekten die vooral arme landen of mensen treffen worden slechts met mondjesmaat ontwikkeld. Veel geld wordt daarentegen gestoken in onderzoek naar zeldzame aandoeningen en minieme verbeteringen in de behandeling van ziekten waar de rijken zich druk om maken. Het geval van alzheimer laat zien dat zulke mechanismen de definities van aandoeningen mee kunnen bepalen en het onderzoek soms ook een doodlopend pad opsturen – en daar gevangen houden.
Wat nu?
Waar moet de evaluatie van het alzheimeronderzoek toe leiden? Dat alzheimer, of we het nu als een ziekte moeten beschouwen of niet, een akelig probleem is zal ieder beamen die de aandoening in zijn of haar directe omgeving heeft meegemaakt. Natuurlijk moeten wij proberen beter inzicht te krijgen in de werking van de hersenen en in de factoren die de werking daarvan verstoren. Maar misschien is het niet slim om zo exclusief in te zetten op het vinden van een silver bullet om het probleem de wereld uit te helpen – in elk geval niet zolang we eigenlijk geen idee hebben wat alzheimer eigenlijk is.
Jacobs en Theunissen wijzen erop dat een biomedische benadering niet alleen zaligmakend hoeft te zijn. Het is niet gezegd dat er voor alzheimer één specifieke oorzaak of één specifieke oplossing is. Sterker, de betiteling van alzheimer als een ziekte heeft ook nadelen, bijvoorbeeld dat mensen op grond van bepaalde symptomen als patiënt kunnen worden betiteld terwijl ze eigenlijk nog heel goed functioneren. Het lijkt verstandig om de biomedische loopgraven te verlaten en ook te kijken naar andere benaderingen die misschien niet onmiddellijk gouden bergen beloven maar praktisch gezien effectiever zijn, denk aan ouderengeneeskunde en openbare gezondheidszorg.
Een eenvoudige oplossing die in één klap alle problemen uit de wereld helpt, lijkt in elk geval ver weg, alle miljarden die daaraan besteed zijn ten spijt. Wetenschap vermag veel, maar is geen winkel van Sinkel waar alles leverbaar is als je maar genoeg betaalt.




